Canlı hücre minyatür bir kimya fabrikasıdır. Bu fabrikanın mikroskobik mekânında binlerce tepkime gerçekleşir.
Örneğin şekerler aminoasitlere çevrilir ya da bunun tam tersi olur. Küçük moleküller polimerleri oluşturacak şekilde birleşirler. Hücrenin gereksinimleri değiştiğinde, bu polimerler hidroliz edilirler.

Organizmada gerçekleşen kimyasal tepkimelerin tümü metabolizma olarak adlandırılır. Bir bütün olarak metabolizma, hücrenin madde ve enerji kaynaklarını idare etmekle görevlidir.
Bazı metabolik yollar büyük molekülleri daha basit bileşikleri yıkarak enerji açığa çıkarırlar. Bu yıkım süreçleri katabolik yollar olarak adlandırılır. ( hücresel solunum tepkimeleri)
Buna karşılık olarak anabolik yollar, daha basit moleküllerden daha karmaşık molekülleri kurmak için enerji kullanırlar. ( aminoasitlerden protein sentezi)
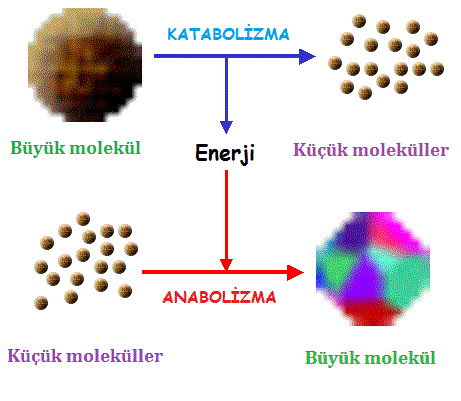
Özetle anabolizma ve katabolizma bir şehrin yokuş aşağı ve yokuş yukarı giden caddeleri olarak düşünülebilir.
Katabolizmanın yokuş aşağı tepkimelerinde açığa çıkarılan enerji, anabolizmanın yokuş yukarı tepkimelerini gerçekleştirmek için kullanılır.
Canlı organizmalar çevreleriyle enerji ve madde alış verişi yapabilen ‘’ açık sistemler ‘’dir. Kapalı sistemlerde madde ve enerji akışı bir müddet sonra ( sistem dengeye ulaştığında ) durur. Yani sürekli değildir.
Termodinamiğin iki yasası organizmalar ve bütün diğer madde birlikteliklerindeki enerji dönüşümlerini yönetir.

Termodinamiğin birinci yasasına göre evrenin enerjisi sabittir.
Enerji aktarılabilir ve dönüştürülebilir, ancak yeniden yaratılamaz ya da yok edilemez.
Örneğin kaydırağa tırmanan bir çocuk besinlerin içerisindeki depolanmış enerjiyi kas kasılmasıyla kinetik enerjiye dönüştürmekte, kaydırağa tırmandığında bu kinetik enerji potansiyel enerjiye dönüşmüş halde olmakta aşağı doğru kayarken ise tekrar kinetik enerjiye dönüşmektedir.
Termodinamiğin ikinci yasasına göre her enerji aktarımı ya da dönüşümü evrenin düzensizliğini artırır. Bu düzensizlik entropi olarak adlandırılır.
Canlı organizmalar enerjilerinin büyük kısmını ısı şeklinde dışarı şeklinde vererek entropilerini düşürmek yani kararlı yapılarını korumak isterler. Her sistem kendi kararlı yapısını oluşturmak isterken evrenin entropisini artırır.

Metabolizmadaki tepkimeler serbest enerji değişikliklerine göre endergonik ve egzergonik tepkimeler olmak üzere 2 şekilde gerçekleşir.
Egzergonik tepkimelerde dışarıya enerji verilir ve sistemin toplam enerjisi düşer. Örneğin oksijenli solunumda glikozun toplam enerjisi solunum ürünleri olan CO2 ve H2O dan 686 kilokalori daha azdır. Daha doğru bir ifadeyle solunum ürünleri olan bu maddeler şeker moleküllerinde depolanmış olan bu enerjiyi bu molekülden uzaklaştıran bir sürecin tükenmiş artıklarıdır.
![]()
Endergonik tepkimelerde ise moleküller serbest enerji depolarlar yani bu tepkimelerin gerçekleşmesi için çevreden enerji soğurulması gerekir. Örneğin fotosentezde karbondioksit ve suyun kendilerinden daha fazla enerjiye sahip şekerlere dönüşebilmesi ışık enerjisi sayesinde mümkün olabilmektedir.
Canlı sistemlerde egzergonik ve endergonik reaksiyonlar arasındaki enerji transferi ATP molekülü sayesinde olmaktadır.
ATP oldukça yüksek enerjili ve kararsız bir moleküldür. Sahip olduğu fosfat bağlarındaki enerjiyi başka moleküle aktararak kendisi kararlı bir hale gelirken fosfat grubunu aktardığı molekülü enerjisini yükseltmek vasıtasıyla aktif hale getirir.
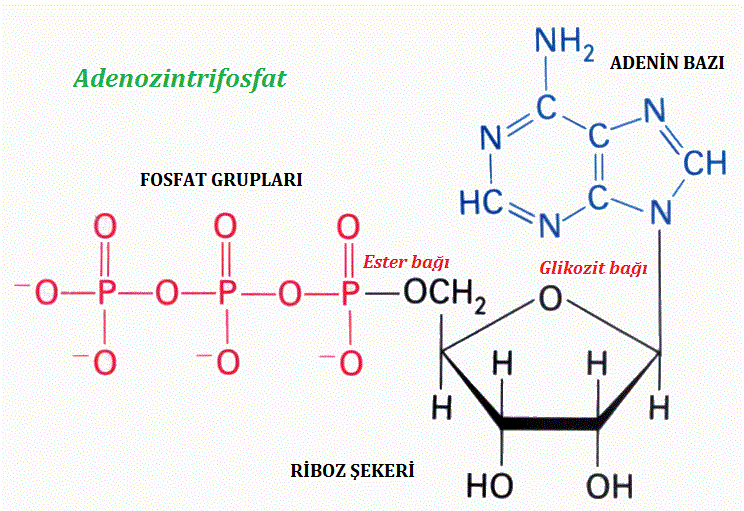
ATP yapısındaki enerjiyi endergonik tepkimelerin gerçekleşmesi için başka moleküllere aktarırken, egzergonik tepkimelerde serbest kalan enerji ATP sentezinde kullanılır.
Canlı hücrelerde ATP sentezine fosforilasyon, ATP yıkımına ise defosforilasyon denir.
Fosforilasyon 3 farklı şekilde gerçekleşebilir.
Substrat düzeyinde fosforilasyon
Enzimatik reaksiyonlarla ATP sentezidir. Oksijenli ve oksijensiz solunumda, fermantasyon süreçlerinde gözlenir. Tüm canlılarda gerçekleşen fermantasyon tipidir.
Oksidatif fosforilasyon
Yükseltgenme indirgenme tepkimeleri neticesinde ATP sentezidir.
Fotofosforilasyon
Işık enerjisiyle ATP sentezidir.
ATP molekülünün yapım ve yıkımı canlı her hücrede her saniye devam eden süreçlerdir.
Örneğin bir kas hücresi saniyede 10 milyon ATP molekülünü yıkar ve yeniden oluşturur. İnsanın günlük ATP üretim tüketimi yaklaşık kendi vücut ağırlığı kadardır.
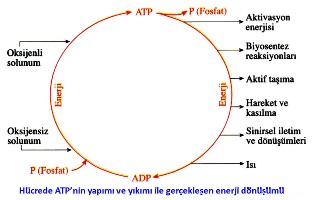
Her kimyasal tepkimenin başlaması için önündeki enerji engelini aşması gerekir. Tepkime egzergonik yani enerji veren bir tepkime dahi olsa bu engel aşılmalıdır.
Aktivasyon enerjisi denen bu enerji, normal dağılım gösteren maddenin içindeki moleküllerin bir kısmının enerjisini yükseltmede, ( çarpışma olasılığının artması ile ) dolayısıyla tepkimeye girmesin sağlamada kullanılır.
Aktivasyon enerjisi engelinin aşılması canlı dışı sistemlerde moleküllerin ısıtılması sayesinde mümkün olabilir. Ancak canlı sistemlerde esas yapının proteinlerden oluşması sebebiyle çok yüksek sıcaklık derecelerine çıkmak söz konusu değildir.
O halde dış ortamda çok yüksek bir aktivasyon enerjisi engelini aşarak gerçekleşen tepkimelerin hücre içinde hücresel yapıya zarar vermeden gerçekleşebilmesi için aktivasyon enerjisi engelinin düşürülmesi gerekir.
Aktivasyon enerjisi engeli canlıların kararlı yapılarını sürdürebilmeleri için son derece önemlidir.
Hücrelerde sentezlenen ve çoğunlukla hücre dışında da etkinliklerini sürdüren, aktivasyon enerjisi engelini düşürerek kimyasal tepkimelerin daha düşük sıcaklık derecelerinde ve daha hızlı gerçekleşmesini sağlayan protein yapılı katalizörlere enzim denir.
Enzimler kimyasal reaksiyonların daha hızlı gerçekleşmesini sağlarlar, ancak tepkimede salınan ya da çevreden alınması gereken enerji miktarını değiştirmezler. Yani enzimi kullanılsa da kullanılmasa da reaktiflerin toplam enerjisi ile ürünlerin toplam enerjisi arasındaki fark daima aynıdır.
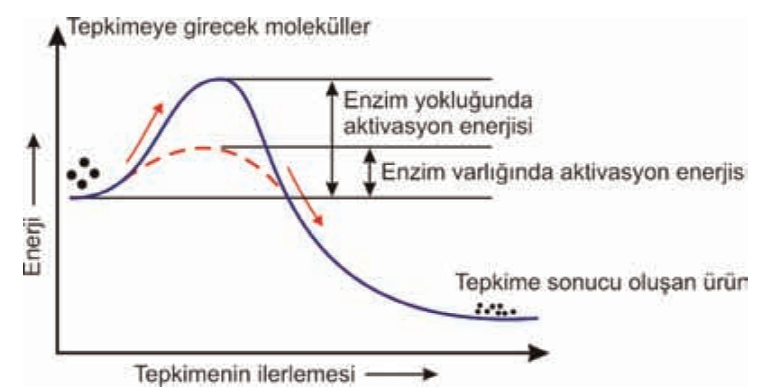
Enzimlerin kimyasal reaksiyonları ne kadar hızlandırdığını anlamak için şu örnek yeterli olur.

Bir Hidrojen peroksit molekülü ( H2O2 ) enzimsiz ortamda 300 senede parçalanabilirken, katalaz enzimi 1 saniyede 5.000.000 H2O2 molekülünü parçalayabilir.
Enzimler yapılarına göre;
- Basit ve
- Bileşik enzim
olmak üzere 2 farklı biçimde olabilirler.
Basit enzimler sadece proteinden meydana gelir. Metabolik aktivite için yardımcı kısma gerek duymaz. Pepsin ve üreaz bu tür enzimlerdir.
Bileşik enzimlerde apoenzim olarak adlandırılan protein kısım yanında, prostetik grup ya da diğer adıyla yardımcı grup ta bulunur.
Apoenzim kısmı enzimin hangi maddeye etki edeceğini belirlerken yardımcı grup ta enzimi çalışır hale getirir.
Yardımcı grup Fe+2 Mn+2 Mg+2 Zn+2 gibi inorganik iyonlardan oluşuyor ise kofaktör, vitaminler ya da nükleotidler gibi organik ise koenzim adını alır.
Apoenzimle yardımcı grup arasındaki ilişki elinde çapa olan bir işçi örneğiyle daha anlaşılabilir hale gelebilir.

Kazılacak yeri belirleyen işçi bileşik enzimde enzimin etki edeceği maddeyi seçen apoenzim kısmıyla, işçiyi çalışır hale getiren çapa ise apoenzimi aktifleştiren yardımcı gruba benzetilebilir.
Bileşik enzimlerin yapısında bulunan apoenzim kısmı sadece tek bir çeşit yardımcı grupla çalışır hale gelebilirken; bir yardımcı grup çeşidi birden fazla apoenzimi aktifleştirebilir. Bu durumda hücredeki apoenzim çeşidi, sayısı yardımcı grup çeşidi sayısından fazla olacaktır.
Kısaca bir işçi tek bir çapa ile çalışabilirken, bir çapa birden fazla işçi tarafından kullanılabilir.
PDF DOSYASI İÇİN
